COSS
kids Nederland
Coalition of Silicone Servivers
RIVM De zorg voor morgen begint vandaag
Tekortkomingen in technische
dossiers siliconen borstimplantaten
09-06-2016
Keizers P, van Drongelen A, de Jong W, van Oostrom C, Roszek B,
Venhuis B, de Vries C, Geertsma R, Janssen R
COSSkids is onderdeel van Coalition of Silicone Servivers - Boulder Collorado USA
2 februari 2017
NOOIT HAD DE LEUGEN EEN
DUIDELIJKER GEZICHT
DUIDELIJKER GEZICHT

Voor medische hulpmiddelen, zoals siliconen borstimplantaten,
zijn fabrikanten verplicht om ‘technische dossiers’ aan te leggen
op basis waarvan wordt bepaald of het product op de markt wordt
toegelaten. De dossiers van 10 fabrikanten die in Nederland
siliconen borstimplantaten op de markt brengen, blijken duide-
lijke tekortkomingen te hebben. Bij laboratoriumonderzoek van
de implantaten zelf zijn geen afwijkingen aangetroffen die de
gezondheid zouden kunnen schaden.
Dit blijkt uit verkennend onderzoek van het RIVM dat in opdracht van
de Inspectie voor de Gezondheidszorg (IGZ) is uitgevoerd.
Hiervoor zijn belangrijke onderdelen van de technische dossiers van
10 fabrikanten van siliconen borstimplantaten tegen het licht gehouden.
Volledige en correcte dossiers zijn essentieel om de kwaliteit en
veiligheid van het hulpmiddel voor de patiënt te waarborgen. Daarnaast
is laboratoriumonderzoek verricht naar de chemische samenstelling en
de mate waarin de implantaten schadelijke eigenschappen hebben.
Uit het laboratoriumonderzoek bleek dat de materialen gebruikt in de producten voldoen aan een internationaal erkende veiligheidstest die schadelijke effecten op cellen meet. Om de biocompatibiliteit van het product als geheel te controleren, zijn aanvullende testen vereist. Chemische analyse liet zien dat twee fabrikanten een andere grondstof hadden gebruikt dan vastgelegd in hun technisch dossier. Omdat het in beide gevallen wel om medische siliconengel gaat heeft dit geen gevolgen voor de patiëntveiligheid. In één implantaat werden relatief hoge concentraties van bepaalde onzuiverheden (cyclosiloxanen) aangetroffen. Deze afwijking heeft naar verwachting geen negatief effect op de patiëntveiligheid.
zijn fabrikanten verplicht om ‘technische dossiers’ aan te leggen
op basis waarvan wordt bepaald of het product op de markt wordt
toegelaten. De dossiers van 10 fabrikanten die in Nederland
siliconen borstimplantaten op de markt brengen, blijken duide-
lijke tekortkomingen te hebben. Bij laboratoriumonderzoek van
de implantaten zelf zijn geen afwijkingen aangetroffen die de
gezondheid zouden kunnen schaden.
Dit blijkt uit verkennend onderzoek van het RIVM dat in opdracht van
de Inspectie voor de Gezondheidszorg (IGZ) is uitgevoerd.
Hiervoor zijn belangrijke onderdelen van de technische dossiers van
10 fabrikanten van siliconen borstimplantaten tegen het licht gehouden.
Volledige en correcte dossiers zijn essentieel om de kwaliteit en
veiligheid van het hulpmiddel voor de patiënt te waarborgen. Daarnaast
is laboratoriumonderzoek verricht naar de chemische samenstelling en
de mate waarin de implantaten schadelijke eigenschappen hebben.
Uit het laboratoriumonderzoek bleek dat de materialen gebruikt in de producten voldoen aan een internationaal erkende veiligheidstest die schadelijke effecten op cellen meet. Om de biocompatibiliteit van het product als geheel te controleren, zijn aanvullende testen vereist. Chemische analyse liet zien dat twee fabrikanten een andere grondstof hadden gebruikt dan vastgelegd in hun technisch dossier. Omdat het in beide gevallen wel om medische siliconengel gaat heeft dit geen gevolgen voor de patiëntveiligheid. In één implantaat werden relatief hoge concentraties van bepaalde onzuiverheden (cyclosiloxanen) aangetroffen. Deze afwijking heeft naar verwachting geen negatief effect op de patiëntveiligheid.
Het blauw onderlijnde gedeelte werd na de vraagstelling van
Zorg.Nu gewijzigd in het orginele verslag.
Zorg.Nu gewijzigd in het orginele verslag.
Reactie op borstimplantaten: IGZ
08-11-2016
Naar aanleiding van de uitzending van Zorg.nu op 8 november 2016, over borstimplantaten, heeft IGZ
onderstaande reactie gegeven.
1. Het RIVM concludeerde in haar onderzoek dat alle technische dossiers van
fabrikanten van siliconen borstimplantaten gebreken vertoonden. Hoe verklaart de
IGZ dit?
In het onderzoek is niet onderzocht waarom de technische dossiers gebreken vertoonden. Het onderzoek toont
alleen aan dat de technische dossiers gebreken vertoonden.
2. Welke vervolgacties verbindt de IGZ hieraan?
De IGZ heeft alle resultaten teruggekoppeld aan elke fabrikant. Daarnaast heeft de IGZ de fabrikanten
opgeroepen om geconstateerde tekortkomingen te verbeteren en hierover contact op te nemen met de
betrokken aangemelde instantie. Ook de betrokken aangemelde instanties zijn door IGZ geïnformeerd over de
onderzoeksresultaten. En ook zij zijn opgeroepen acties te ondernemen die leiden tot verbetering van de
technische dossiers en de kwaliteitsborging. Daarnaast heeft de IGZ de Europese lidstaten waar de fabrikanten
en/of aangemelde instanties gevestigd zijn geïnformeerd over de onderzoeksresultaten. Deze lidstaten kunnen
de verbetermaatregelen van de fabrikanten en aangemelde instanties in de gaten houden. Samen met de
Europese lidstaten heeft de IGZ een Europese werkgroep opgezet om ervoor te zorgen dat de
verbetermaatregelen worden doorgevoerd.
3. Is er contact geweest met fabrikanten van siliconen borstimplantaten over de
gebreken die de technische dossiers vertonen?
Zie antwoord bij vraag 2.
4. Is er contact hierover geweest met de betreffende Notified Bodies, zijn hier
consequenties aan verbonden voor hun werkwijze, zo ja, welke?
Zie antwoord vraag 2. In aanvulling hierop kan de IGZ aangeven dat er voor dit specifieke geval geen
consequenties zijn verbonden aan de huidige werkwijze van de betrokken aangemelde instanties.
Als gevolg van het Joint Plan for Immediate Action (van EU-commisioner Dalli) uit 2012 is het toezicht op notified
bodies versterkt. Notified bodies worden nu door een Europees inspectieteam beoordeeld. Dit heeft tot gevolg
gehad dat al diverse notified bodies hun taken hebben neergelegd of het aantal verschillende type
hulpmiddelen dat zij mogen beoordelen ingeperkt is.
De uitkomsten van dit onderzoek zijn daarom ook gedeeld met het Joint Assessment Team dat de gezamenlijke
inspecties aan notified bodies begeleidt, zodat hier in het toezicht aandacht aan besteed kan worden.
5. Hoe kunnen incomplete technische dossiers de veiligheid van patiënten
waarborgen?
Vraag gesteld aan het ministerie van VWS ‘Wat zijn heel concreet de
'borgingspunten' bij de 'ontwikkeling en productie van implantaten'?’ (brief
minister d.d. 9 juni 2016)
Tekortkomingen in het technische dossier hoeven niet direct te leiden tot een onveilig product. Veel van de
gevonden tekortkomingen zijn administratief van aard. Bijvoorbeeld een protocol verwijst niet naar bepaalde
testen die uitgevoerd zijn of informatie over accessoires bij of varianten van de implantaten ontbreekt. Ook als
deze accessoires of varianten er niet zijn, moet dat vermeld worden. Verder heeft het RIVM regelmatig
gevonden dat bepaalde risico’s wel in de gebruiksaanwijzing genoemd staan, maar niet in de risicoanalyse. De
risico’s zijn dus wel in beeld en er wordt voor gewaarschuwd, maar ze moeten ook vastgelegd zijn in de
risicoanalyse. Daarnaast heeft het RIVM kritisch gescoord op informatie over het systeem voor Post-Market
Surveillance (PMS). IGZ is van mening dat fabrikanten actief ervaringen met hun producten bij gebruikers
moeten verzamelen en analyseren. Hierop kritisch geoordeeld, bijvoorbeeld of in de procedure manieren
genoemd zijn om deze informatie te verzamelen en wat hier vervolgens mee gebeurt. Als deze informatie
ontbrak in het dossier is dit als afwezig (negatief) beoordeeld.
Wanneer er tekortkomingen zijn in het technisch dossier kan de fabrikant nog wel een veilig product hebben,
alleen heeft hij dit niet compleet onderbouwd in het dossier. Daarnaast zijn er meer punten waarop een
fabrikant wordt beoordeeld die de veiligheid van het product en daarmee ook de patiëntveiligheid kunnen
borgen.Het kwaliteitsmanagementsysteem wordt bijvoorbeeld beoordeeld door de aangemelde instantie en
daarnaast voeren aangemelde instanties ook audits uit om fabrikanten te toetsen.
Wel is het door een tekortkoming in het technisch dossier mogelijk dat er voor bepaalde risico’s niet voldoende
beheersmaatregelen worden genomen, waardoor de risico’s niet tot een minimum worden beperkt. Zie ook
antwoord vraag 2. Hierbij moet wel benadrukt worden dat een medisch hulpmiddel nooit 100% veilig is, er zijn
altijd risico’s aan het gebruik van een medisch hulpmiddel verbonden. Het uitgangspunt is dat er een goed
evenwicht bestaat tussen de gezondheidsbaten van het medisch hulpmiddel en de risico’s die de toepassing
daarvan met zich meebrengt.
6. Wat zijn de gevolgen van de aangetroffen verhoogde cyclosiloxanen voor de
veiligheid van de patiënt en op basis van welk relevant onderzoek concludeert de
IGZ dit?
De IGZ wil benadrukken dat de verhoogde concentratie cyclosiloxanen is aangetroffen bij 1 implantaat van 1
fabrikant. Naar verwachting heeft deze bevinding geen invloed op de patiëntveiligheid. De concentratie
cyclosiloxanen die is gemeten voor dit onderzoek is vergelijkbaar met de concentratie die in PIP implantaten is
gemeten waarvan de Europese onderzoekscommissie SCHEER (Scienfitic Committee on Health, Environmental
and Emerging Risks - voorheen SCENIHR) heeft aangegeven dat deze hoeveelheden niet als risico voor de
patiëntveiligheid worden beschouwd. Zie ook het rapport 'The safety of poly implant prothese silicone breast
implants - Update of the opinion of February 2012' van SCHENIHR.
Hoewel het betreffende implantaat in 2009 is gefabriceerd beschouwt de inspectie de aanwezigheid van
dergelijke concentraties niet als state-of-the-art, omdat andere borstimplantaten uit dezelfde periode wel
zonder detecteerbare niveaus aan cyclosiloxanen geproduceerd zijn. Implantaten van latere productiedata van
dezelfde fabrikant bevatten geen detecteerbare niveaus van cyclosiloxanen. De partij waar dit implantaat uit
komt is inmiddels niet meer op de markt, omdat de houdbaarheidsdatum is verlopen. Gezien de eerdere
rapporten van SCENIHR acht de inspectie preventief verwijderen van deze implantaten niet aangewezen, omdat
de risico van een operatie veel groter zijn.
7. Het RIVM concludeert (p. 33 RIVM report 2015-0100) dat er aanvullend
onderzoek nodig is op het gebied van biocompatibiliteit, wie houdt hier toezicht op?
De notified body houdt hier toezicht op, zij beoordelen dit onderdeel van het technisch dossier ten behoeve van
afgifte van het CE-certificaat. De IGZ en haar collega autoriteiten uit de andere lidstaten houden weer toezicht op
de notified bodies. Via de Europese werkgroep die de IGZ naar aanleiding van dit rapport in het leven heeft
geroepen zal zij het belang van onderzoek naar biocompatibiliteit en het toezicht hierop door de notified body
benadrukken en verbeteringen op dit onderwerp monitoren.
8. Hoe verloopt het IGZ onderzoek naar de 200 meldingen m.b.t. siliconen
borstimplantaten?
Persbericht van IGZ van 7 oktober. Zodra er meer bekend is over dit onderzoek zal IGZ dit communiceren via de
website.
9. De Franse ANSM heeft fabrikanten van siliconen borstimplantaten een deadline
gegeven om missende biocompatibiliteitsdata uit technische dossiers alsnog aan te
dragen, met mogelijke consequenties van dien. Wat doet de IGZ op dit punt?
De IGZ onderhoudt nauw contact met de Franse toezichthouder over het onderzoek dat zij uitvoeren. De Franse
toezichthouder onderzoekt hierbij ook technische dossiers van fabrikanten die siliconen borstimplantaten
leveren op de Nederlandse markt.
In de market surveillance studie is ook het onderdeel biocompatibiliteit van de technische dossiers beoordeeld.
De fabrikanten zijn op dit moment bezig om verbeteringen aan te brengen in de technische dossiers, het
onderdeel biocompatibiliteit wordt indien nodig meegenomen met deze verbetermaatregelen. In opdracht van
de IGZ zal het RIVM vervolgonderzoek uitvoeren, Het onderdeel biocompatibiliteit wordt hierin meegenomen.
10. De Franse INCa concludeerde eerder dat er een duidelijk link bestaat tussen
ALCL en siliconen borstimplantaten. Wat concludeert de IGZ hieruit?
Vraag gesteld aan het ministerie van VWS 'Hoe staat het met het onderzoek naar de veiligheid van siliconenborst
implantaten en ALCL in Europees verband?'
Zie onze website met Q&A’s over borstimplantaten.
Discrepantie door RIVM aangetroffen gelvulling borstimplantaten
In haar rapport 'Silicone breast implants in the Netherlands. A market surveillance study' concludeert het RIVM
dat voor fabrikanten SBI06 en SBI08 de door het RIVM aangetroffen gel niet overeenkomt met de gel die de
fabrikant aangeeft te gebruiken. In het geval van SBI06 blijkt dit op een misverstand te berusten. SBI08 heeft
aangegeven dat de conclusie van het RIVM onjuist is. Met deze fabrikant wordt nog een gesprek gepland om dit
nader te verifiëren.
Discrepantie aangetroffen gelvulling SBI06 berust op misverstand
IGZ en RIVM hebben na publicatie van het rapport overleg gehad met fabrikant SBI06. Zij hebben toen
aannemelijk kunnen maken dat zij inderdaad de gel gebruiken die het RIVM heeft aangetroffen. De fabrikant had
echter per abuis in het technisch dossier een 'technical specification sheet' van een ander type (eveneens
medical grade) siliconengel toegevoegd. Uit andere documentatie in het technisch dossier, de sectie van de
beschrijving van het implantaat, bleek inderdaad dat zij het type (medical grade) gel gebruiken dat het RIVM
heeft aangetroffen. Dat dit type gel aan fabrikant SBI06 is geleverd, is bevestigd door NuSil Technologies, de
toeleverancier van het siliconen basismateriaal. Er is hier dus geen sprake meer van een discrepantie.
SBI08 geeft aan een ander type medische siliconen te gebruiken
Het RIVM heeft een discrepantie gevonden in de gel die het RIVM op basis van onderzoek verwachtte aan te
treffen en de gel waarnaar SBI08 in het technisch dossier verwijst. Volgens SBI08 is de toegepaste siliconengel,
Applied Silicone PN 40008, equivalent aan de samenstelling van de siliconengel waarnaar het technisch dossier
verwijst (40004). Het RIVM zal aanvullende informatie hierover bestuderen. Er is overeengekomen om
voorafgaand hieraan met SBI08 in overleg te gaan.
Implantaat met verhoogd niveau cyclosiloxanen
Het RIVM rapport geeft tevens aan dat het implantaat met de verhoogde concentratie cyclosiloxanen van deze
fabrikant is: 'It is noted that the implant containing the impurities is also one of the
implants of which the experimentally determined gel deviates from the type listed in
the technical file. However, the number of implants investigated is too limited to state
whether the over-all quality of products from SBI08 are less than those of the
products of the other manufacturers.'
Zoals in ons eerdere antwoord aangegeven ging het om één implantaat. Van deze fabrikant zijn meerdere
implantaten op cyclosiloxanen onderzocht van latere productiedata, maar ook van een vergelijkbare
productiedatum. In geen van deze implantaten zijn meetbare cyclosiloxanen aangetroffen.
In reactie op de vraag over het verhoogde niveau van cyclosiloxanen in een implantaat geproduceerd in 2009,
geeft de inspectie aan: 'De partij waar dit implantaat uit komt is inmiddels niet meer op de markt, omdat de
houdbaarheidsdatum is verlopen.'
Op de vraag van Zorg.nu hoeveel implantaten in deze partij zaten, kan de inspectie geen antwoord geven. Deze
informatie is niet bekend bij de inspectie en hoeft dat ook niet te zijn. Dit is de verantwoordelijkheid van de
fabrikant. De resultaten van dit ene implantaat zeggen daarnaast ook niets over of de rest van de partij is
aangedaan. Daarvoor zou de hele partij onderzocht moeten zijn. Om welke fabrikant het gaat, kan de inspectie
niet zeggen, omdat de resultaten in het rapport geanonimiseerd zijn weergegeven. De identiteit betreft dus
vertrouwelijke informatie.
Risico’s voor patiëntveiligheid niet verwacht
Er zijn twee toeleveranciers van siliconen van medische kwaliteit: Applied Silicone en NuSil Technology. Deze
toeleveranciers voeren zelf ook onderzoeken uit naar de biocompatibiliteit van de siliconen. Deze testen voeren
zij uit conform de daarvoor geldende norm (ISO 10993). Dat neemt niet weg dat fabrikanten zelf ook testen naar
biocompatibiliteit moeten uitvoeren. Daarvoor heeft het RIVM tekortkomingen in de technische dossiers
aangetroffen. Hiervan verwacht het RIVM echter geen risicio’s voor de patiëntveiligheid, het rapport zegt
hierover (paragraaf 2.11, pagina 19):
'The shortcomings found for 'device description' and 'biocompatibility' cause little concern because they are of
administrative nature, respectively are counterbalanced by the available information. The negative outcome for
biocompatibility is primarily caused by not correctly following procedures to decide on which tests are needed.
However, they did perform a standard set of tests according to applicable standards and the results did not
indicate problems.'
Wat betreft de gels die in het onderzoek in de implantaten zijn aangetroffen, zegt het RIVM rapport op pagina 28:
'With regard to the type of gel, discrepancies were found for two suppliers [waarvan
in ieder geval voor SBI06 dit berust op een misverstand, zie boven. IGZ] between the
experimentally determined type and the information in the technical file. These
shortcomings will not have an impact on patient safety, since these types of gels are
of medical grade.'
Dit is dus niet vergelijkbaar met de situatie van PIP, waarbij industriële siliconen werden gebruikt.
De inspectie heeft bekend gemaakt dat er een onderzoek komt naar de klachten van vrouwen met siliconen
borstimplantaten door het RIVM. De vrouwen die zich als eerder hadden aangemeld bij stichting SVS zullen door
de stichting gevraagd worden vooral mee te werken aan het RIVM onderzoek. Naast de bestaande lijst van
vrouwen die zich hebben gemeld heeft de stichting ook nieuwe meldingen ontvangen. Deze vrouwen ontvangen
ook een oproep. De inspectie zal dan tevens vrouwen gaan oproepen die zich niet bij de SVS hebben gemeld,
maar wel borstimplantaten hebben (gehad). Dit kan betekenen dat het onderzoek groter wordt, omdat de
nieuwe aanmeldingen van vrouwen ook worden meegenomen.'

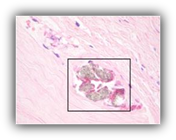
Study bewijst: Siliconen migreren door het gehele lichaam.
Kijk ook op UITZENDING GEMIST op Zorg.Nu van 8 november 2016 over de rol van IGZ-RIVM.
Sorry voor de reclame.
Sorry voor de reclame.
VERVOLG uitzending ZorgNu Avrotros 15-11-2016
Reactie van de Nederlandse Vereniging van Plastische Chirurgen NVPC van 15-11-2016
Dit mocht niet bekend worden tijdens het programma van Antoinette Hertzenberg op 8 november 2016:
Cyclic volatile methylsiloxanes
in human blood as markers for
ruptured silicone gel-filled
breast implants.
Onder de knop het verslag en de Nederlandse vertaling
Onder de knop het pathologisch onderzoek van Dr. Plastisch Chirurg Rita Kappel, patholoog Henri Dijkman en Lucas de Boer.
Study proves:
silicone found in the whole body!
silicone found in the whole body!
Click the link below for the Dr. Kappel study in the English lanquest:
Studie erklärt: Silikon im ganzen Körper gefunden
Klicken Sie auf den Link oben für die Studie von Dr. Kappel in der englischen Sprache:
Het kalf is verdronken, IGZ/RIVM redden wat nog te redden is! De antwoorden op de vragen van Antoinette Hertzenberg in Zorg.Nu. van 8 en 15 november 2016. Beschermend zijn de antwoorden zeker, jazeker....voor de producenten van siliconen borstimplantaten maar zeker niet voor de slachtoffers!
Het begrip "Medical Grade" voor Siliconen?
Voor de productie van sliconen-implantaten berust op een kwinkslag van Dow Courning die nergens op is geba-seerd.
Dow Courning gebruikte voor zijn productie "Industrial Grade" siliconen en veranderde zelf de naam op het etiket in "Medical Grade". Wetenschappers die om technische specificaties vroegen kregen het volgende te horen:
"Er bestaat geen algemene overeenstemming over de normen voor de standaard van het implantaat van siliconen elastomeren, of voor andere toepassingen".
Met andere woorden "Medical Grade" is een sprookje, een leugen om vrouwen als proefkonijnen voor chemicalien te kunnen gebruiken tot de dood er op volgt.
Voor de productie van sliconen-implantaten berust op een kwinkslag van Dow Courning die nergens op is geba-seerd.
Dow Courning gebruikte voor zijn productie "Industrial Grade" siliconen en veranderde zelf de naam op het etiket in "Medical Grade". Wetenschappers die om technische specificaties vroegen kregen het volgende te horen:
"Er bestaat geen algemene overeenstemming over de normen voor de standaard van het implantaat van siliconen elastomeren, of voor andere toepassingen".
Met andere woorden "Medical Grade" is een sprookje, een leugen om vrouwen als proefkonijnen voor chemicalien te kunnen gebruiken tot de dood er op volgt.